Perché i muscoli aumentano di tono dopo un buon programma di allenamento professionalmente strutturato? Perché il petto gonfia, le spalle si allargano, i glutei si alzano e le braccia diventano sagomate? E soprattutto qual è la causa di quel dolore ai muscoli il giorno dopo? E perché “guariamo” miracolosamente dopo un paio di giorni? Ovviamente non parleremo di acido lattico, ormai questo mito è sfatato da anni. Per chi è fresco di fitness, tranquilli, non è l’acido lattico che si accumula per giorni. La risposta a tutte queste domande è da ricercare nelle cellule satelliti.
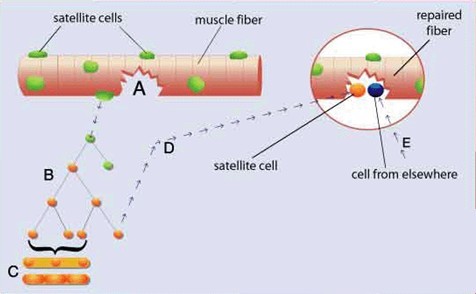
Le cellule satelliti (CS) sono le più abbondanti cellule staminali del muscolo scheletrico. Esse sono ampiamente riconosciute per il loro contributo al mantenimento della massa muscolare, la rigenerazione e l'ipertrofia durante la durata della vita umana. Queste cellule sono delle ottime candidate per la terapia cellulare grazie alla loro capacità di auto-rinnovamento e alla loro multi-capacità di differenziazione. Le ritroviamo in abbondanza tra la lamina basale delle miofibre e la membrana plasmatica (Fig 1). Esse svolgono un ruolo importante nell’ipertrofia e nella rigenerazione muscolare dove intervengono mediante l'aggiunta dei nuclei delle CS alle fibre muscolari esistenti. La popolazione delle CS inoltre detiene una grande riserva nucleare tale da consentire la rigenerazione muscolare; tuttavia, la loro mitosi è solitamente quiescente. In questo periodo, la letteratura scientifica ci suggerisce che sia stimoli fisiologici sia patologici, influenzano potenzialmente l’attivazione delle CS, la proliferazione e la differenziazione. L'attivazione di tali cellule avviene a seguito dell'esercizio fisico. Com’è noto dopo l’allenamento si creano delle micro-lesioni al livello delle fibre muscolari scheletriche.
Secondo la ricerca del Professor Behzad Bazgir et Al. qui descritta, diverse modalità di allenamento determinano effetti diversi. Quest’articolo tenterà di descrivere l’impiego delle CS da parte dell’organismo nella rigenerazione muscolare e nell’ipertrofia.
Una volta attivato il processo, le CS si auto-rinnovano per fornire una popolazione di cellule indifferenziate e dormienti pronte a ripartire nel caso di un successivo danno cellulare.
Fig. 1 https://musolino.jimdo.com/neverpressed/science/come-cresce-un-muscolo
Come vengono attivate le cellule satellite?
Quando un muscolo scheletrico è sottoposto a stress (allenamento) o leso per un trauma, le CS escono dal loro stato di quiescenza e si attivano. In seguito proliferano, si differenziano e si fondono in miofibre preesistenti creando nuovi mionuclei o se in eccesso tornare allo stato basale di quiescenza.
Esistono poche informazioni sul meccanismo molecolare che sta alla base del suddetto processo. Per motivi di spazio, limitiamoci a scrivere che il tutto è regolato da una famiglia di proteine chiamate miogeniche (MRFs, Myf-5, MyoD) che ne controllano l’attivazione, la progressione e fungono da feedback come marcatori terminali (Fig 2).
Fig. 2 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5086326/bin/Cell-J-18-473-g01.jpg
Le CS in risposta a diversi tipi di stimoli o sotto il controllo di MRF possono essere attivate, possono proliferare, essere differenziate e infine partecipare alla rigenerazione muscolare. In assenza di MRF, tuttavia, diverse fasi del ciclo di vita delle CS possono essere bloccate o inibite.
Quando si attivano le cellule satellite?
Le CS sono mitoticamente quiescenti e il loro stato è alterato in risposta ad una varietà di stimoli fisiologici e patologici come la denervazione, l’invecchiamento, la sarcopenia, le ustioni, la vasocostrizione prolungata in caso d’ipotermia e, ultimo ma non per ultimo, l’esercizio fisico. Dall’altra parte, condizioni patologiche come distrofia muscolare di Duchenne ed esposizione alle radiazioni possono incidere sulla quiescenza delle CS, sul loro numero, sull'attivazione e sullo stato di differenziazione attraverso molteplici vie di segnalazione. I fattori regolatori del loro comportamento includono elementi presenti nel loro microambiente circostante che racchiude gli elementi strutturali, quali le miofibre, i fattori secreti dalle cellule interstiziali, la micro vascolarizzazione, le giunzioni neuromuscolari, le cellule immunitarie e fattori sistemici quali insulin-like, l’ossido nitrico (NO), il fattore di crescita-1 (IGF-I) e il fattore di crescita degli epatociti (HGF), quest'ultimo è stato recentemente associato a un ruolo scatenante l’attivazione delle CS.
Ma cos’è l’ipertrofia e come sono coinvolte le cellule satelliti in questo processo?
La fisiologia ci suggerisce che le CS oltre alla genesi di fibre muscolari scheletriche stimolano l’ipertrofia muscolare, ossia un aumento delle dimensioni delle fibre muscolari scheletriche, che si verifica durante l'allenamento ed è un processo complesso e interessante attraverso diversi siti e fattori stimolatori/inibitori al livello delle giunzioni neuromuscolari. Secondo la teoria, un aumento del muscolo scheletrico si verifica solo in concomitanza di un incremento sostanziale della sezione trasversale delle miofibre. La teoria del dominio nucleare afferma che questo complemento cellulare si verifica nei primi anni di crescita giovanile attraverso un espansione, per l'appunto, del "dominio cellulare". Questa teoria implica che alterazioni nel numero dei mionuclei avvengono attraverso almeno due meccanismi:
1) l'aggiunta di mionuclei, ad opera delle CS, durante l’ipertrofia
2) da un declino di mionuclei durante l'apoptosi (morte cellulare programmata) e/o necrosi durante l’atrofia delle fibre muscolari.
Tuttavia gli studi hanno rilevato che l’intervento delle CS avviene sia nei giovani sia nei soggetti anziani sottoposti ad allenamento. È interessante notare inoltre che questa risposta è dipendente dal genere. L’allenamento contro resistenza (RT) sembra dare risultati scientificamente significanti di stimolo-risposta ipertrofica CS-indotta solo nei soggetti volontari maschi.
È scientificamente rilevante il ruolo della miostatina e dei mioblasti, come due dei più potenziali fattori di crescita inibitori d’ipertrofia muscolare. La miostatina sopprime MyoD e aumenta la capacità di auto-rinnovamento delle CS mantenendole in stato quiescente. Anche se l'inibizione della miostatina induce ipertrofia muscolare, questo processo sembra essere CS-indipendente. Essendo l’ipertrofia muscolare e il rimodellamento processi complicati, ulteriori studi in corso d’opera, stanno spostando l’attenzione sul ruolo relativo per tutta la durata della vita sia in stati fisiologici (sesso, giovinezza, invecchiamento e RT) sia in condizioni patologiche come la sindrome di Duchene (distrofia muscolare). Il processo di rigenerazione muscolare è costituito da tre fasi: lisi, riparazione e rimodellamento. Ogni fase è controllata da molteplici fattori regolatori autocrini. Tuttavia, le CS sembrano svolgere un essenziale ruolo nel processo di rigenerazione muscolare, soprattutto nelle ultime due fasi di riparazione e rimodellamento. La ricerca è limitata a causa di considerazioni etiche e difficoltà nell'ottenere CS sufficienti per innesti in soggetti distrofici e nel reclutare volontari per l’espianto e il trapianto di CS. Inoltre l’ingegneria e la tecnologia medica attuale rende impossibile l’espianto di Queste cellule in soggetti viventi. La letteratura attualmente si basa su studi in vitro e/o su topi da laboratorio. Ed è proprio secondo la ricerca di Collins et al., che i risultati sul trapianto di CS provenienti da topi sani su tessuto muscolare scheletrico di topi con distrofia muscolare sembrano evidenziare una rigenerazione del pool di SC e un aumento della rigenerazione della fibra muscolare. La ricerca però evidenzia anche che il tessuto muscolare scheletrico dei roditori e degli uomini, presenta sostanziali differenze. Primo perché è diversa la quantità di CS presenti tra uomo e topo, secondo perché la capacità di rigenerazione del muscolo di topo sembra essere indipendente dalla loro ubicazione.
La compatibilità uomo/roditore invece sembra trovare riscontro tra i vari attivatori che possono influenzare il ciclo di vita delle CS e la loro capacità di partecipare alla rigenerazione muscolare come i fattori di crescita, quali IGF-1, il fattore inibitorio della leucemia (LIF),l’HGF e il fattore di crescita endogeno dei mioblasti (FGF) che induce rigenerazione dei mioblasti negli esseri umani e nei topi. Tuttavia, isoforme diverse dei fattori di crescita hanno differenti effetti in contrasto con IGF-1 e IGF-6 che hanno un effetto di soppressione sulla rigenerazione muscolare indotta delle CS.
Allenamento e attivazione delle cellule satellite
È stato chiaramente dimostrato che l'attività muscolare aumenta la proliferazione delle CS, mentre l'inattività muscolare ne diminuisce la proliferazione. L'esercizio fisico può essere facilmente intrapreso da chiunque e suoi parametri manipolati (frequenza, intensità, durata, volume e tipo/modalità di esercizio) quindi questo può essere un non-farmaco naturale rigenerativo. Anche se è giusto ricordare che l'esercizio fisico, inteso come stress fisiologico, potrebbe potenzialmente esercitare effetti modulatori durante le diverse fasi del ciclo di vita delle CS. Come si vede nella Tabella 1, differenti allenamenti possono modulare l'attivazione delle CS in vari modi.
Tuttavia, resta ancora complicata la determinazione del volume esatto, la durata e la soglia di esercizio fisico per l'attivazione ottimale delle CS in soggetti diversi con diversi livelli d’idoneità fisica, età e sesso.
 |
Cellule satellite e allenamento di endurance
Le CS si attivano, come ampiamente detto finora, come risposta a eventi quali le micro-lesioni che seguono l’esercizio fisico. Variazioni nel contenuto e nell'attività delle CS dopo l'allenamento di endurance possono essere attribuite a differenze d’intensità, durata e frequenza dell'esercizio somministrato e/o in parte ai muscoli interessati. Il tempo e l'intensità dell’allenamento sono importanti fattori che contribuiscono l’attivazione delle CS. Un incremento nel contenuto cellulare è stato segnalato tra i 40 e i 155 minuti di allenamento a moderata/alta intensità, mentre negli allenamenti a bassa intensità non è stato rilevato alcun cambiamento anche dopo oltre i 40 minuti. Questa scoperta ha comportato che l'intensità dell'esercizio è un fattore importante nell’attivazione delle CS e supporta un impegno nella rigenerazione muscolare.
Varie sono le conclusioni di questi studi. In generale occorre sapere che un aumento nel contenuto di CS dipende dall'intensità piuttosto che dalla durata poiché i vari gruppi muscolari reagiscono in modo diverso anche nello stesso programma di allenamento. Il contenuto delle CS nei topi da laboratorio non aumentava se non dopo una settimana di allenamento su un tapis roulant per 30 minuti al giorno. I risultati diventano significativi dopo 2-4 giorni di attività sul tapis roulant.
Altre ricerche chiariscono però che alcuni studi si sono basati sul muscolo soleo (noto per essere principalmente un muscolo lento che possiede livelli di CS maggiori a riposo ed è meno sensibile alla stimolazione rispetto ai muscoli veloci mentre altri sul muscolo tibiale anteriore.
Com’è noto, le fibre di tipo I hanno più CS rispetto a quelle di tipo II e quindi un minore potenziale adattivo. Infine, sembra giocare un ruolo decisivo il tipo di contrazione muscolare che può modulare la risposta delle CS.
Si è registrato un aumento del numero di CS 72 ore dopo aver somministrato ai roditori 90 minuti di tapis roulant con inclinazione in eccentrica di -13.5°.
In uno studio di Eksteen, in cui dei corridori ben allenati, completando 10 sessioni ad elevata intensità in un protocollo di 4 settimane in discesa (-6˚) e in salita (+ 15˚), si evidenzia una risposta nella proliferazione delle CS nel muscolo vasto laterale segnata da un aumento CD56 (138%) e M-caderina (123%). In tale studio sia in salita sia in discesa l’aumento di miogenina è stato significativamente rilevante, interpretato in percentuale, da un notevole 56% (in salita) e 60% (in discesa).
Risposta delle cellule satellite tra allenamento contro resistenza (macchine e pesi liberi) e stimolazione elettrica
Il metodo migliore e più rapido per osservare una risposta delle CS in un programma RT a breve termine è il metodo in eccentrica (ECC-RT) su muscoli superficiali e accessibili testati con un semplice Hand grip isocinetico. Un confronto tra ECC-RT e stimolazione elettrica in 8 soggetti giovani ha dimostrato che la stimolazione elettrica ha determinato un elevato aumento della miogenina 24 ore dopo l'allenamento. Tuttavia, lo studio ha mostrato incrementi simili di CD56 e Pax7 a 24, 96, e 192 ore dopo il semplice allenamento ECC-RT.
Anche qui appare chiaro che l’intensità sembra giocare un ruolo chiave nel modificare positivamente e negativamente la risposta delle CS verso l'RT. Ci sono ampi risultati a sostegno dell'efficacia di un allenamento a intensità moderata/elevata, anche con uso d’integratori per lo sport.
Quello che al momento sembra rimanere ignoto è la determinazione di una soglia minima d’intensità necessaria per l'attivazione delle cs, anche se alcune prove hanno dimostrato che, anche a bassa intensità, l’RT potrebbe stimolare l’attivazione.
Recentemente si è anche studiato come a bassa intensità [20-30% di una ripetizione massima (1 RM)] la stenosi muscolare (BFR) stimoli positivamente marcatori come (CD56, PAX7, MyoD). Quello che appare certo al momento è che allenamenti strutturati a lungo termine inducano effetti diversi ma pur sempre positivi sia sulla struttura sia sulla funzione muscolare.
Allenamento contro resistenza e integratori per lo sport
Un certo numero di studi pubblicati mostrano gli effetti dell’allenamento a lungo termine con uso d’integratori sulle CS. Alcuni sostengono che con 6-20 settimane di allenamento e uso d’integratori, aumenti sia il numero di CS sia l’attivazione (Tabella 1). La Durata dell’RT somministrato variava all'origine dello studio da 30 a 64 sedute a intensità moderata/elevata (60-80% 1 RM). Bellamy et al. in particolare indagano sugli effetti delle proteine del siero del latte in un programma RT total body di16 Settimane (64 sessioni) ad alta Intensità (75-80% 1 RM). I risultati pubblicati hanno evidenziato che il protocollo di allenamento ha indotto un aumento del 47% di CS nel post training.
Allenamento di endurance (ET) VS allenamento di contro resistenza (RT)
Pochi studi comparativi hanno evidenziato la risposta delle CS a lungo termine tra RT ed ET. Vi sono risultati che testimoniano un incremento simile sia nei muscoli deltoidi sia nel vasto laterale dopo 14 settimane di RT (7 w) e di ET (7 w) negli stessi soggetti. Anche se a causa delle diverse composizioni del tipo di fibra muscolare, il confronto è stato poco razionale. Anche qui l'intensità gioca un ruolo principale. Confrontando gli effetti di tre intensità di RT (al 90% 1 RM a cedimento, al 30% 1 RM a cedimento e il 30% con il 90% 1 RM) si evidenzia che le percentuali di CS aumentano in tutti e tre i gruppi, considerando però che aumenti di MyoD e miogenina si riscontrano solo nel gruppo al 30% 1RM a cedimento. Gli autori hanno suggerito che la bassa intensità e l’alto volume nell’RT sono tra i più potenti stimoli anabolizzanti a discapito dei sostenitori dell’alta intensità a basso volume. Questi risultati hanno suggerito che esiste realmente un volume di allenamento ottimale e come tale, la fatica è uno stimolo significativo per l'attivazione, la proliferazione e la differenziazione delle CS. Da notare, inoltre che la simultanea stimolazione di RT ed ET aumenta significativamente il numero di CS con conseguente aumento della massa muscolare e dei mionuclei. Tuttavia, l’esercizio di endurance da solo potrebbe non aumentare il contenuto di CS, né in numero dei mionuclei e delle miofibre né nei processi di attivazione.
Questo concetto è importante nella prescrizione dell’esercizio fisico per i pazienti anziani che soffrono di debolezza muscolare (vale a dire, l'invecchiamento, la sarcopenia e le altre condizioni patologiche), dove la crescita della massa muscolare e la ripresa funzionale del muscolo hanno una priorità speciale.
Tutte le fibre muscolari reagiscono allo stesso modo?
Sembra che le differenti miofibre diano risposte differenti sull’attivazione delle CS. Sebbene alcune evidenze dimostrano che miofibre di tipo I e II abbiano lo stesso contenuto di CS, numerosi studi rivelano che le fibre di tipo I possiedono un numero maggiore di CS latenti sia nei roditori sia nell'uomo. Mentre le fibre di tipo II hanno un’attività aumentata di CS. Questo processo sembra ragionevole poiché le fibre di tipo II danno un maggiore contributo alla massa muscolare (ipertrofia) e quindi una capacità di risposta superiore all’RT. Tuttavia, questa ipotesi ha bisogno di un chiarimento futuro.
In conclusione possiamo affermare che i meccanismi di allenamento che inducono un’attivazione delle CS non sono completamente identificati. Tuttavia, quello che è chiaro, è che l'esercizio induce micro-lesioni, usura e lacerazione del tessuto muscolare scheletrico, dove le risposte infiammatorie compensative portano all'attivazione delle CS. Tuttavia, dati recenti hanno mostrato che non c’è attivazione di CS dopo un allenamento a bassa intensità poiché il danneggiamento cellulare non è significativamente importante, mentre allenamenti di potenza, possono alterare regolatori autocrini, endo e para (Fig.2) e come, è già ben noto, l'esercizio fisico aumenti i livelli sistemici di CS che controllano le citochine, gli ormoni endocrini e i fattori di crescita.
Infine, diversi tipi di allenamento (in particolare le contrazioni eccentriche) possono imporre sollecitazioni meccaniche e danni al sarcolemma. L’esercizio fisico può influenzare regolatori negativi delle CS, compresi miostatina e fattore di crescita trasformante beta (TGF-β). L’esercizio fisico è altresì indicato per fermare effetti inibitori della miostatina sulle CS. L’incremento dell’attività delle CS è registrato anche dopo programmi a breve termine, ma aumenta in numero esponenziale solo dopo aver seguito programmi a lungo termine di RT ed ET. Sono però necessarie nuove ricerche per chiarire l'esatto ruolo distintivo e interattivo tra allenamento e fattori normativi delle CS al fine di evidenziare i meccanismi coinvolti nell'adattamento muscolare per condizioni patologiche quali per esempio la distrofia muscolare. Riassumendo quindi, ricordiamo che: le CS sono le più importanti cellule staminali presenti nel muscolo scheletrico. Esse diminuiscono con l’invecchiamento, la sarcopenia e le malattie neuromuscolari come la distrofia muscolare.
Al contrario, stimoli fisiologici come RT ed ET inducono micro-lesioni muscolari che in seguito daranno inizio ad adattamenti compensativi positivi sia tramite un aumento del numero di CS sia dalla soppressione della riduzione del contenuto delle CS per invecchiamento. Modalità di esercizio, volume, intensità e durata devono essere perfettamente ottimizzati per attivare, far proliferare e consentire la differenziazione delle CS.
Questi sono considerati temi caldi in argomento “cellule staminali ed esercizio fisico”. Alcuni studi suggeriscono che l'intensità dell'esercizio è il fattore più importante che determini l'attivazione, mentre altri sostengono che è il volume che gioca un ruolo essenziale. Nel loro insieme, una soglia ottimale determina nei vari protocolli di esercizio la giusta stimolazione.
A cura di
| dott. Francesco Vella |
 |
| dott. Umberto Li Vigni |
Il presente articolo si è ispirato a “Satellite Cells Contribution to Exercise Mediated Muscle Hypertrophy and Repair” Behzad Bazgir, Ph.D., Rouhollah Fathi, Ph.D., Mojtaba Rezazadeh Valojerdi, Ph.D. Paul Mozdziak, Ph.D., Alireza Asgari, Ph.D.
Bibliografia
- Bankol LC, Feasson L, Ponsot E, Kadi F. Fibre type specific satellite cell content in two models of muscle diseases. Histopathology. 2013; 63(6): 826-832.
- Petrella JK, Kim JS, Cross JM, Kosek DJ, Bamman MM. Efficacy of myonuclear addition may explain differential myofiber growth among resistance-trained young and older men and women. Am J Physiol Endocrinol Metab. 2006; 291(5): E937-946.
- Kadi F, Thornell LE. Concomitant increases in myonuclear and satellite cell content in female trapezius muscle following strength training. Histochem Cell Biol. 2000; 113(2): 99-103.
- Kosek DJ, Kim JS, Petrella JK, Cross JM, Bamman MM. Efficacy of 3 days/wk resistance training on myofiber hypertrophy and myogenic mechanisms in young vs. older adults. J Appl Physiol. 2006; 101(2): 531-544.
- Amthor H, Otto A, Vulin A, Rochat A, Dumonceaux J, Garcia L, et al. Muscle hypertrophy driven by myostatin blockade does not require stem/precursor-cell activity. Proc Natl Acad Sci USA. 2009; 106(18): 7479-7484.
- Crameri RM, Aagaard P, Qvortrup K, Langberg H, Olesen J, Kjaer M. Myofibre damage in human skeletal muscle: effects of electrical stimulation versus voluntary contraction. J Physiol. 2007; 583(1): 365-380.
- Shefer G, Rauner G, Yablonka-Reuveni Z, Benayahu D. Reduced satellite cell numbers and myogenic capacity in aging can be alleviated by endurance exercise. PLoS One. 2010; 5(10): e13307.